Aktuelt
Genriving i blinde
Snart kan genklippende celler settes inn i mennesker. Det er ikke sikkert det er trygt.
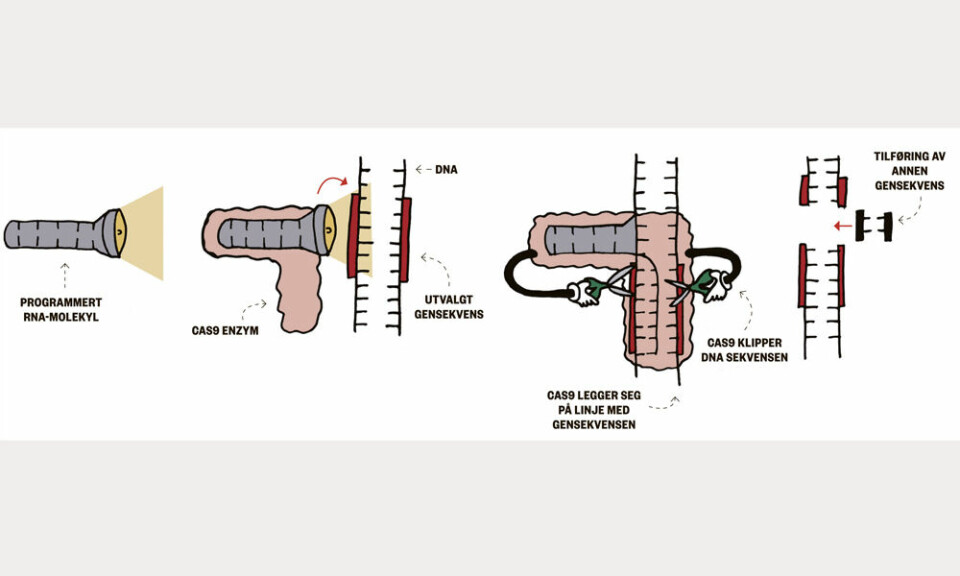
For første gang er en studie som skal bruke genteknologien CRISPR-Cas9 på mennesker, godkjent i USA.
Teknologien har fått enorm oppmerksomhet siden den ble oppdaget i 2014. Ved å bruke enzymet Cas9 kan forskerne «klippe bort» enkeltgener som forårsaker blindhet, kreft og en rekke andre sykdommer. En etisk komité godkjente i juni en studie som skal teste genredigerte celler i kreftpasienter.
– Det overrasker meg, kommenterer Simon Dankel ved Universitetet i Bergen, som forsker på teknologien i samarbeid med Harvard-forskerne som først brukte den på menneskeceller.
Hittil har den etiske diskusjonen rundt CRISPR vært mest fremtredende: Kan teknologien brukes til å lage designbabyer i fremtiden? I essayet i herværende avis ber medisinerne Bjørn Hofmann og Henrik Vogt oss om å stoppe og tenke på slike spørsmål. Men la den delen ligge et øyeblikk: Er teknologien i det hele tatt så trygg som entusiastene skal ha det til?
– Det virker tidlig å begynne med slike studier på mennesker, sier Dankel.
Riv riktig hus. Det varJ. Keith Joung, en Harvard-professor som selv forsker på CRISPR, som ropte varsku på et møte om genredigering i Washington i midten av juli: Er forskerne som strutsen, som stikker hodet i sanden for å slippe å se faren i det de gjør i øyene? Joung er bekymret for det som kalles off-target-effekter:
Et gen er en bokstavrekke i DNA-tråden, en viss kombinasjon av syremolekylene som betegnes med A, T, C eller G. CRISPR retter seg mot en bestemt slik sekvens og klipper den bort. Problemet er at vi kan ha samme gen, samme sekvens, flere steder i DNA-et.
Det er som om noen ber deg rive huset i Kirkegata 6, men glemmer å si om de mener i Oslo, Hønefoss eller Vardø.
– Man ønsker å endre nøyaktig det vi tror er årsak til sykdom. Selv i celleeksperimenter blir vi utfordret på dette: Vet dere om behandlingen kun treffer det genet dere er interessert i? sier Simon Dankel, som med sine kolleger i Bergen bruker CRISPR til å undersøke fedmegener i museceller.
– DNA er dessuten aldri helt likt i to personer. Når du skal gjøre en CRISPR, må du designe det som heter guide-RNA som bare passer med DNA-et man vil treffe. Det varierer fra person til person, sier han.
Det er umulig å si generelt hva som vil skje om CRISPR fjerner flere DNA-deler enn det som var meningen. Det kan være ingenting, eller det kan gjøre pasienten dødssyk – det kommer an på genet som fjernes.
– Man vet ikke hvor mange slike off-target-effekter en behandling kan gi. Poenget er at risikoen er tilstede. Da må man kartlegge den grundig, sier Dankel.
Spørsmål om suksess. Den godkjente studien skal etter planen bruke CRISPR til å endre genene i T-celler, en slags immunforsvarscelle. Forskerne, tilknyttet University of Pennsylvania, vil endre cellene slik at de blir i stand til å gjenkjenne og angripe tre typer kreftceller. Cellene skal så settes inn i blodet til pasienter med uhelbredelig kreft.
Studien er en såkalt klinisk fase 1-studie, den skal kun sjekke at behandlingen er trygg – at den ikke gjør pasientene dårligere eller dreper dem. Eventuelle oppfølgingsstudier vil så måtte avgjøre om behandlingen fungerer.
– De tenker vel at gevinsten for pasienter som ikke har noe håp, er større enn risikoen for eventuelle bieffekter, sier Dankel.
Studien må fortsatt godkjennes av det amerikanske tilsynet FDA før den kan settes i gang. To andre team konkurrerer med forskerne i Pennsylvania om å bli de første til å bruke CRISPR i mennesker. Kinesiske forskere har fått godkjent en tilsvarende T-cellestudie, og et team i delstaten Massachusetts vil teste metoden på en type genetisk blindhet. Prestisjen vil være stor for dem som først kan vise til (positive) resultater.
Men hvordan vurderes suksess? Hvor stor oppbremsing av en sykdom er godt nok til at behandlingen kan testes videre? Hvor store bivirkninger er for store?
– Om dette er første steg, blir terskelen kanskje lavere for å utvide godkjenningen til andre tilfeller av menneskelig genmanipulering, sier Dankel.

















